Eines der faszinierendsten Gebiete der kernchemischen Grundlagenforschung ist die Untersuchung der chemischen Eigenschaften der nur in Schwerionenreaktionen zug├żnglichen, k├╝nstlichen Elemente jenseits der Actiniden, der Transactiniden. Dabei interessiert sich der Kernchemiker nicht nur f├╝r die nuklearen Eigenschaften dieser Elemente, sondern auch f├╝r ihre chemischen Eigenschaften und damit f├╝r deren Einordnung in das Periodensystem der chemischen Elemente. Beginnend mit den Elementen 104, 105, 106 bilden sie diejenigen ├£bergangsmetalle, in denen die 6d-Elektronenschale aufgef├╝llt wird. Somit sind diese Elemente schwere Homologe der Elemente Hafnium, Tantal, Wolfram, d.h. sie stehen im Periodensystem in derselben Gruppe wie diese und sollten dieselbe Valenzelektronenkonfiguration besitzen. Nun haben die Transactinidenelemente aber einen wesentlich h├Čher geladenen Atomkern, der bewirkt, dass die Elektronen der H├╝lle st├żrker als bei den leichten Homologen beschleunigt werden. So soll das 1s-Elektron von Element 104 etwa 76% der Lichtgeschwindigkeit, bei Element 106 bereits 77% und bei Element 118 (Eka-Radon) sogar 86% der Lichtgeschwindigkeit besitzen [Per00]. Dieser Effekt, der proportional zum Quadrat der Kernladungszahl ansteigt, bewirkt eine relativistische Massenzunahme des Elektrons, die sich auf die Anziehungskr├żfte der Elektronen durch den Kern und somit auf die r├żumliche Struktur der Orbitale auswirkt. Dies f├╝hrt zu einer Ver├żnderung der Lage der Energieniveaus im Atom und damit gegebenenfalls zu einer ver├żnderten Valenzelektronenkonfiguration (Abbildung 1).
Neben der experimentellen Herausforderung, mit diesen nur k├╝nstlich zug├żnglichen Elementen zu arbeiten, ist es reizvoll zu erfahren, ab welcher Kernladungszahl die relativistischen Effekte einen wesentlichen Einfluss auf das chemische Verhalten dieser Elemente aus├╝ben und ob die Einordnung in das Periodensystem der Elemente ab einer bestimmten Kernladungszahl v├Čllig anders vorgenommen werden muss. Relativistische Effekte sind bereits im ŌĆ×normalenŌĆ£ chemischen Alltag und mit blo├¤em Auge, z.B. beim Gold, zu beobachten [Scw94]. Die Absorption von Licht der Energie hn = 2,4 eV f├╝r Gold kann durch den ├£bergang vom gef├╝llten 5d-Energieniveau in das (6s) Fermiband beschrieben werden. Die relativistisch berechnete Energiedifferenz betr├żgt 2,38 eV. F├╝r Silber ist die entsprechende relativistische Anhebung des 4d-Orbitals und die Absenkung des 5s-Orbitals viel geringer, und die Absorption tritt erst bei etwa 3,7 eV auf, also im ultravioletten Bereich. Bei nichtrelativistischen Rechnungen w├żre Gold wei├¤, wie Silber [Pyy88, Eli94]. Die Tatsache, dass der ├£bergang von 5d106s1 zu 5d96s2 parit├żtsverboten ist, f├╝hrt dazu, dass freie Goldatome eigentlich transparent (und auch nicht gelb) sein sollten, obwohl die Farbe des Metalls von den Atomeigenschaften herr├╝hrt. Auf die Unterschiede zwischen dem Verhalten einzelner Atome (wie es f├╝r die Chemie der Transactiniden typisch ist) und der Chemie von Makromengen wird sp├żter eingegangen werden.
F├╝r das erste Transactinidenelement mit der Kernladungszahl 104 (Rutherfordium, Rf) ist das Energieniveauschema in Abbildung 1 gezeigt. Relativistische Rechnung zeigen eine so gro├¤e Absenkung des 7s-Orbitals und eine so gro├¤e Anhebung des 6d-Orbitals, dass das 7s-Orbital energetisch unter den 6d-Orbitalen liegt. Nichtrelativistische Rechnungen geben diesen Trend nicht wieder. Bei den leichten Homologen Zr, Hf und dem Pseudohomologen[1] Th zeigen erwartungsgem├ż├¤ die relativistischen Rechnungen keine so starken Ver├żnderungen in der Elektronenkonfiguration.
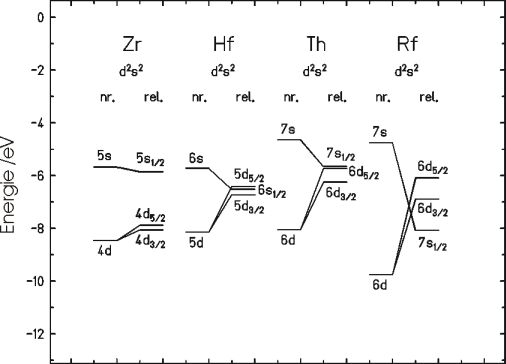
Abb.1 Energieniveauschema f├╝r Rutherfordium und seine Homologen Hf, Zr und das Pseudohomologe Th, berechnet mit relativistischen (rel.) und nichtrelativistischen (nr.) Methoden [Per00]
Die mit atomaren Wellenfunktionen zu beschreibenden makroskopischen, atomaren und molekularen Eigenschaften werden durch relativistische Effekte stark ver├żndert. Ein Vergleich der radialen Elektronendichtefunktionen nichtrelativistischer (Hartree-Fock-Slater-Methode) und relativistischer Rechnungen (Dirac-Slater-Methode) ist in [Per93, Per96, Per99] zu finden. Durch die ├änderung der r├żumlichen Ladungsverteilung der Elektronen werden atomare Eigenschaften wie Ionisationspotentiale und Atom- bzw. Ionenradien beeinflusst. Auswirkungen auf molekulare Eigenschaften sind die Kontraktion der Bindungsl├żngen, die Stabilit├żt der maximalen Oxidationsstufen, die relativen und absoluten Verschiebungen der Energieniveaus, die Einfluss auf die Stabilit├żt der Molek├╝le und die Bindungsart haben. Als Ma├¤ f├╝r die St├żrke des kovalenten oder ionischen Bindungscharakters dient der Wert der totalen ŌĆ×overlap populationŌĆ£ bzw. die effektive Ladung.
Somit k├Čnnen einerseits experimentelle Ergebnisse zum chemischen Verhalten der Transactiniden einen Beitrag zur Pr├╝fung der theoretischen Voraussagen leisten, andererseits k├Čnnen experimentelle Ergebnisse durch den Vergleich zu relativistischen MO-Rechnungen besser verstanden und interpretiert werden.
Die experimentelle Herausforderung resultiert aus den extrem niedrigen Produktionsraten f├╝r diese schweren Elemente, die nur in Schwerionenreaktionen an Beschleunigern zug├żnglich sind. F├╝r die meisten Arbeiten zur Untersuchung von Transactiniden wird ein Target aus einem langlebigen Actinide, z.B. Curium-248 (T1/2 = 3,40 * 105 a) genutzt, welches in einer Weltproduktion von j├żhrlich nur 150 mg vor allem am Hochflussreaktor in Oak Ridge speziell f├╝r die Grundlagenforschung hergestellt wird.
Wegen der sehr kleinen Bildungsraten im Nano- bzw. Picobarnbereich (siehe unten), der kurzen Halbwertszeiten und der experimentell beschr├żnkten Targetdicken werden bei den heute an modernen Beschleunigern erreichbaren Strahlstr├Čmen weniger als ein Atom pro Minute f├╝r Rutherfordium bzw. ein Atom pro Stunde f├╝r Seaborgium gebildet. Die Chemie, die dabei untersucht wird, ist demnach eine Chemie einzelner Atome (One-Atom-at-a-Time Chemistry [Hof93]), die es mit der Chemie von Makromengen zu vergleichen gilt. Hierbei ist nicht nur der Unterschied im Verhalten von Tracermengen und Makromengen prinzipiell neu (siehe sp├żter), zugleich ist die Signifikanz gro├¤er Zahlen mehr als nur eine Frage der Nachweisbarkeit in der Chemie: Gro├¤e Zahlen sind die Grundlage f├╝r den statistischen Zugang zum Verst├żndnis chemischer Reaktionen als dynamische, reversible Prozesse. Dass diese Grundlage f├╝r chemische Reaktionen einzelner Atome wegf├żllt und welche Konsequenzen daraus erwachsen, wird sp├żter diskutiert.
Die verwendete Methodik f├╝r chemische Experimente mit Transactiniden l├żsst sich im wesentlichen in zwei Gruppen von schnellen Separationstechniken einteilen: Die Trennung bzw. Untersuchung in der Gasphase und in der w├żssrigen Phase. Die Gaschemie liefert vor allem thermodynamische Daten, wie Verdampfungs- und Adsorptionsenthalpien bzw. -entropien. Die Untersuchung in der w├żssrigen Phase liefert Informationen ├╝ber Komplexbildung (und Hydrolyse), wobei sich drei verschiedene Systeme etabliert haben: Die offline Batchtechnik (ŌĆ×SRAFAPŌĆ£ [Her88]), die Ionenaustausch- bzw. Extraktionschromatographie mit ARCA (siehe sp├żter) und die Trennung ├╝ber zum Teil mehrere, hintereinander geschaltete Fl├╝ssig-Fl├╝ssig-Extraktionsstufen mit dem SISAK-System [Per89]. Mit dieser Arbeit soll eine neue Untersuchungs┬Łmethode etabliert werden, die online Chromatographie mit der Mehrs├żulentechnik.
Bei einer online (englisch gebr├żuchlicher: on-line/ off-line) Methode werden die in der Kernreaktion erzeugten Atome kontinuierlich aus der Targetkammer ausgetragen, in die w├żssrige Phase ├╝berf├╝hrt und ├╝ber das Chromatographiesystem gesp├╝lt. Im Gegensatz dazu werden bei der offline Methode die erzeugte Atome f├╝r eine bestimmte Zeit gesammelt und dann in die w├żssrige Phase ├╝berf├╝hrt, also diskontinuierlich verarbeitet.
Mit zunehmender Kernladungszahl werden im allgemeinen die Halbwertszeiten der zur Verf├╝gung stehenden Isotope der Elemente immer k├╝rzer und die Produktionsraten immer kleiner. Das hei├¤t zum einen, dass der Transport des in einer Kernreaktion entstehenden Nuklids zur Chemieapparatur, die Sammelzeit bei offline Technik, die chemische Untersuchung und insbesondere die Probenpr├żparation immer schneller durchgef├╝hrt werden m├╝ssen. Zum zweiten nimmt die Experimentierdauer f├╝r ein signifikantes Ergebnis stark zu. Der Trend geht deshalb zu kontinuierlich, online arbeitenden Systemen. Ferner bedingt die rapide abnehmende Produktionsrate, dass die Detektion des Transactinids gegen St├Črsignale immer besser diskriminiert werden muss. Die signifikante Detektion ist aber nicht nur eine Frage der chemischen Trennung mit hohen Dekontaminationsfaktoren, sondern sie stellt auch hohe Anforderungen an die Detektorsysteme und die Diskriminierung gegen nat├╝rliche Radioaktivit├żt und H├Čhenstrahlung.
Die in bisherigen Experimenten mit den Elementen 101, 103, 104, 105 und 106 erfolgreich eingesetzte Chemieapparatur ARCA arbeitet diskontinuierlich. F├╝r die ersten beiden Transactinidenelemente Rutherfordium (Element 104) und Dubnium (Element 105) konnten mit diesem Instrument gute Ergebnisse erzielt werden, da die zur Verf├╝gung stehenden Isotope dieser Elemente ausreichend lange Halbwertszeiten haben und mit hohen Produktionsraten gebildet werden. Die erste Untersuchung zur w├żssrigen Chemie von Seaborgium (Element 106) wurde mit ARCA als einstufige Elution von einer Kationenaustauschers├żule in 5*10-4 M HF/0,1 M HNO3 durchgef├╝hrt [Sc├ż97]. Dieses Experiment demonstrierte, dass sich Seaborgium wie Wolfram und Molybd├żn als neutraler oder anionischer Oxofluoro-Komplex eluieren l├żsst und damit nicht dem Uran ├żhnelt. In diesem Experiment waren waren knapp 4000 Einzelexperimente notwendig, um 3 korrelierte Ereignisse der 265Sg-Tochter261Rf zu detektieren. Die vermutete Spezies l├żsst sich mit SgO2F2 oder SgO2F3- angeben.
In einem sp├żteren Experiment mit Seaborgium wurde der Einfluss der Fluoridionen n├żher untersucht und in einem Hydrolyseexperiment 265Sg ├╝ber einen Kationenaustauscher in 0,1 M HNO3 (ohne HF) eluiert [Sc├ż98]. Dabei eluierte das online mitproduzierte Wolfram von der S├żule, aber es wurden keine Seaborgium-Ereignisse registriert, obwohl 5 a-a-Korrelationen unter den Experimentbedingungen zu erwarten gewesen w├żren.
Ein Verteilungskoeffizient, Kd-Wert, konnte in diesen Experimenten mit ARCA nicht bestimmt werden. Hierzu w├żren wesentlich mehr Einzelexperimente notwendig gewesen.
Bei einem kontinuierlich arbeitenden Chromatographiesystem mit der sogenannten Mehrs├żulentechnik wird nun der direkte Nachweis des Transactinids aufgegeben, und die Retentionszeit des Transactinids in einem chromatographischen System wird ├╝ber die Menge der w├żhrend der Retentionszeit radioaktiv zerfallenen Atome bestimmt. F├╝r diese Methode ist eine geeignete Zerfallskette notwendig, wie sie in der a-Zerfalls┬Łkette des 265Sg (T1/2=7,4 s) zur Verf├╝gung steht. Diese endet beim langlebigen 253Es (T1/2=20 d), welches ├╝ber lange Experimentzeiten akkumuliert werden kann und somit die geringen Ereignisraten kompensiert.
Neben der apparativen Entwicklung zur online ├£berf├╝hrung der mittels Gasjet angelieferten Aktivit├żten in die w├żssrige Phase ist f├╝r diese Methode eine praktisch vollst├żndige Abtrennung der Zerfallsprodukte vor der chemischen Untersuchung des Transactinids durch eine hochwirksame Filters├żule essenziell. Die Methode ist zudem an enge Grenzen bei der Auswahl des chemischen Systems gekn├╝pft, was umfangreiche Kenntnisse zur tr├żgerfreien Chemie der Homologen erfordert. F├╝r diese Voruntersuchungen wurde in dieser Arbeit die ARCA erfolgreich eingesetzt.
Der Nachweis von wenigen Atomen des langlebigen 253Es durch a-Spektroskopie (gegen den elektronischen und nat├╝rlichen Untergrund) f├╝r die abschlie├¤ende Auswertung stellt hohe Anforderungen an das Messsystem.
2.1 Bildungsquerschnitte und nukleare Daten der Transactiniden
Die Produktion schwerer Elemente in w├żgbaren Mengen durch Neutroneneinfang und anschlie├¤endem b--Zerfall endet beim Fermium-256, das ausschlie├¤lich durch Spontanspaltung zerf├żllt. Die Synthese schwererer Elemente gelingt nur noch in Reaktionen mit Schwerionen an Beschleunigern. Dabei m├╝ssen hochgeladene Projektile die Coulombabsto├¤ung des Atomkerns ├╝berwinden, um zu fusionieren, was mit einem rapiden Abfall der Wirkungsquerschnitte (und damit der Produktionsraten) im Gegensatz zum Einfang eines ungeladen Neutrons durch den Atomkern einhergeht (Abbildung 2).
Ab Z=101 k├Čnnen die Elemente nur noch als einzelne Atome produziert werden. Die Produktionsrate f├╝r heute typische Strahlintensit├żten liegt bei 1 Atom pro Minute f├╝r Wirkungsquerschnitte in der Gr├Č├¤enordnung von 1 nb; f├╝r die schwersten Transactiniden f├żllt sie auf 1 Atom pro Monat (Wirkungsquerschnitt ~ 1 pb) ab.
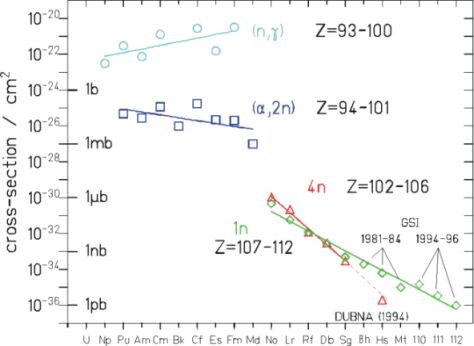
Abb. 2: Wirkungsquerschnitte gegen Z f├╝r verschiedene Bildungsreaktionen (mit freundlicher Genehmigung von Prof. G. M├╝nzenberg, GSI)
Die verwendeten Fusionsreaktionen haben unterschiedliche Konzeptionen. So k├Čnnen neutronenreichere und langlebige Isotope der Elemente 102 bis 108 bevorzugt durch hei├¤e Fusionsreaktionen unter Verwendung von Actinidentargets hergestellt werden. Die Anregungsenergie des gebildeten Compoundkerns (von etwa 40-50 MeV) wird weitgehend durch die Emission von (meist vier bis f├╝nf) Neutronen abgegeben. Eine andere M├Čglichkeit sind kalte Fusionsreaktionen, bei der besonders stabile Targetkerne eingesetzt werden, um den ŌĆ×K├╝hlungseffektŌĆ£ der hohen Bindungsenergie dieser ŌĆ×magischenŌĆ£ bzw. ŌĆ×doppelt magischenŌĆ£ Kerne zu nutzen. Dabei werden mittelschwere Target-/Projektil-Kombinationen genutzt, wie sie z.B. bei der ersten Synthese des heute schwersten Elements 118 (Eka-Radon) in einem Beschuss von Blei-208 mit Krypton-Ionen [Nin99] verwendet wurden. Bei diesen Reaktionen, die auch zur Entdeckung der Elemente 107-112 bei der GSI in Darmstadt f├╝hrten [Hof99, Hof00], ist der Anteil der Spaltung gegen├╝ber dem Prozess der Neutronenemission etwas verringert. Es bilden sich aber sehr neutronenarme, und damit kurzlebige Isotope der schwersten Elemente, die f├╝r chemische Untersuchungen aufgrund der kurzen Halbwertszeit[2] wenig geeignet sind.
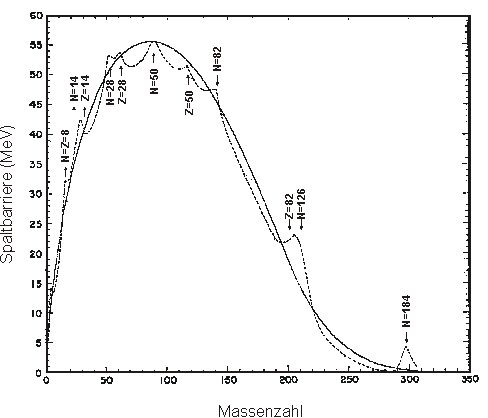
Abb. 3: Stabilit├żt gegen Spontanspaltung bei zunehmender Atommasse ŌĆō aus Myers/Swiatecki [Mye66]
Abbildung 3 zeigt anschaulich, dass mit steigender Masse bzw. dem Quadrat der Kernladungszahl, Z2, die Halbwertszeit nach dem Tr├Čpfchenmodell immer k├╝rzer wird. Bereits bei den leichten Elementen zeichnet sich aber eine ├£berlagerung von Schaleneffekten bei sogenannten magischen Schalenabschl├╝ssen ab. Die Entwicklung der Transactiniden-Forschung ist nun wesentlich von dem Gedanken einer Insel von ŌĆ×Superschweren ElementenŌĆ£ [Mye00, Mye00a] getragen (Abbildung 3).
Das sind Elemente, bei denen durch Schalenstabilisierung die Spontanspaltung so sehr behindert wird, dass sie wieder Halbwertszeiten von Jahren (mindestens jedoch Stunden) haben sollen. In diesem Kontext sind auch die Entdeckungen des Isotops 283112 mit einer Halbwertszeit von 81 +200ŌĆō35 s [Oga98] und des Isotops 298114 mit einer Halbwertszeit von 30,4 s in Dubna[3] [Oga99] einzuordnen, die jedoch kontrovers diskutiert werden [Hof98, Arm00, Hof00].
Durch die theoretischen Arbeiten von Smolanczuk [Smo99], die keine weitere Verringerung der Wirkungs- querschnitte mit Z voraussagen und zur Entdeckung von Element 118 gef├╝hrt haben, sowie durch die Entwicklung von ŌĆ×radioactive beam facilitiesŌĆ£, die neutronenreichere Projektile verwenden [Hof00a, Sc├ż99], um l├żngerlebige Isotope der schwersten Elemente zu bilden, erlebt die Transactinidenforschung derzeit eine Renaissance.
F├╝r Chemieexperimente sind die abnehmenden Produktionsraten dabei nicht an sich das Problem, sondern insbesondere die Bildung von schweren Actiniden durch Transfer┬Łreaktionen und die in geringsten Verunreinigungen im Target enthaltenen schwereren Elemente, die mit dem Projektil kurzlebige Poloniumisotope bilden, welche wie die Transactiniden hochenergetische a-Teilchen emittieren.
Zur Diskriminierung bei der Detektion des eigentlichen Transactinids sind entweder chemische Reinigungsschritte (mit sehr hohen Dekontaminationsfaktoren) notwendig, oder die Diskriminierung ├╝ber geeignete Korrelationsmessung innerhalb einer Zerfallskette. Letzteres wird dabei m├Čglicherweise bei l├żngeren Halbwertszeiten (von mehreren Minuten oder gar Stunden) durch zuf├żllige Korrelationen gest├Črt.
Halbwertszeiten von mindestens einigen Sekunden sind jedoch notwendig, damit das Isotop w├żhrend der chemischen Operationen und der Probenpr├żparation nicht zerf├żllt. Dabei sind Grenzen bei der Kinetik der Komplexbildung und bei der Wechselwirkung mit der Ionenaustauschermatrix oder mit dem Extraktionsmittel zu beachten.
F├╝r eine hohe Nachweiseffizienz sollte ein Isotop des zu untersuchenden Elements zur Verf├╝gung stehen, dessen Zerfallsart (vorrangig a-Zerfall) und Energie der emittierten Strahlung m├Čglichst weitab vom st├Črenden nat├╝rlichen Unter┬Łgrund liegt, damit es gegen St├Čreinfl├╝sse diskriminiert werden kann.
Nur wenn ein Isotop von einem Element zur Verf├╝gung steht, welches sowohl mit signifikant h├Čherer Produktionsrate gegen├╝ber Transferprodukten gebildet wird und entsprechende Halbwertszeiten und Zerfallseigenschaften ausweist, ist es f├╝r chemische Experimente geeignet.
2.2 Eindeutige Identifizierung von Transactiniden
Bei der Entdeckung neuer Elemente wird die Zerfallskette ├╝ber r├żumliche und zeitliche Koinzidenzen (m├Čglichst ├╝ber ein bekanntes Endprodukt) nachgewiesen, nachdem der Produktkern vom Anteil der unerw├╝nschten Kernreaktionsprodukte ├╝ber Masse und Ladung durch physikalische Methoden abgetrennt wurde. Die unerw├╝nschten Transfer┬Łprodukte, mit einem Anteil weit ├╝ber 99,999%, werden ├╝ber Geschwindigkeitsfilter, wie SHIP bei GSI [Mue79], VASSILISSA in Dubna [Yer94] oder mit Hilfe eines gasgef├╝llten Separators [Arm71] abgetrennt. Diese physikalischen Systeme eignen sich im Prinzip auch f├╝r die Ankopplung eines Chemieexperiments: Im Massenseparator erfolgt die sehr schnelle Separation des gew├╝nschten Transactinids und in der anschlie├¤enden Chemieapparatur wird das reine Transactinid chemisch untersucht. Dies bedeutet f├╝r die Detektion des Transactinids einen wesentlich geringeren Untergrund.
Diese interessante M├Čglichkeit wird derzeit am BGS (Berkeley Gas-filled Separator [Nin99a]) sowohl f├╝r SISAK getestet, als auch f├╝r die Untersuchung von Element 108 in der Gasphase vorbereitet.
Bei GSI soll das Projekt SHIPTRAP [Dil00] realisiert werden. SHIPTRAP besteht aus einer nach dem Igisol-Prinzip arbeitenden Puffergaszelle und einer Ionenfalle hinter dem Geschwindigkeitsfilter SHIP [Mue79], die kernphysikalische und physikalisch-chemische Untersuchungen von Elementen mit Z>106 und Halbwertszeiten von T1/2<100 ms erm├Čglichen soll [GSI97]. Das Projekt befindet sich derzeit im Aufbau.
Bei chemischen Experimenten werden die Zerfallseigenschaften durch hochaufgel├Čste Detektion des a-Zerfalls oder der Spontanspaltung (sf) genutzt. F├╝r eine g├╝nstige Diskriminierung gegen den nat├╝rlichen und elektronischen Untergrund bieten sich hierf├╝r die a-a- bzw. a-sf-Korrelationen an. Die kurzen Halbwertszeiten der Transactiniden erweisen sich dabei als g├╝nstig, da der Zerfall des Tochternuklids innerhalb einer kurzen Zeit erfolgt. F├╝r diese Messungen sind PIPS-Detektoren ├╝blich. Der Zeitaufwand und die G├╝te der Probenpr├żparation ist hierbei der entscheidende Faktor bei der Untersuchung sehr kurzlebiger Isotope. Grenzen der a-Spektrometrie setzen der nat├╝rliche und elektronische Untergrund. Vorteilhaft ist die hohe Energie der von kurzlebigen Transactiniden emittierten a-Strahlung, da in diesem Bereich des Spektrums der Untergrund durch nat├╝rliche a-Strahler sehr gering ist. Bei der w├żssrigen Chemie erweist sich jedoch der Zeitaufwand f├╝r die Probenpr├żparationen als der wesentliche Faktor.
2.3 Gasjet-Technik
Produkte, die sich in Kernreaktionen mit geladenen Teilchen bilden, werden wegen der Impulserhaltung aus einem d├╝nnen Target herausgeschleudert. Diese hochgeladenen R├╝cksto├¤kerne k├Čnnen als geladene Ionen in elektrischen und magnetischen Feldern abgelenkt und damit transportiert werden. Dies wird beispielsweise bei SHIP und beim BGS (siehe oben) genutzt, um erw├╝nschte von unerw├╝nschten Reaktionsprodukten sehr effektiv zu trennen.
Werden die R├╝cksto├¤kerne in einem Gasraum abgebremst, lagern sie innerhalb von Bruchteilen einer Sekunde Elektronen aus dem umgebenden Gas an, um ihre hohe Ladung zu verlieren. Dann kann ein Gasjetsystem zum schnellen Transport kurzlebiger Nuklide von der Targetkammer zur Untersuchungsapparatur genutzt werden [Mac69, Puu73, Mac74, Far77, Geo78, Hir80, Ste80]. Diese Technik ist f├╝r online Experimente zur chemischen Untersuchung von in Schwerionenreaktionen gebildeten kurzlebigen Elementen geeignet. Die Targetkammer wird w├żhrend der Bestrahlung st├żndig mit einem Gasstrom durchsp├╝lt, dem Aerosolpartikel beigemengt sind. An diese Aerosolen lagern sich die R├╝cksto├¤atome an und werden so mit dem Gasstrom transportiert. Als Transportgas wird entsprechend der Gr├Č├¤e der Targetkammer Helium, Stickstoff oder Argon eingesetzt, da die Reichweiten der R├╝cksto├¤atome in diesen Gasen unter┬Łschiedlich sind. F├╝r Experimente zur w├żssrigen Chemie wird als Aerosol vorrangig KCl verwendet. F├╝r die Gaschemie haben sich MoO3 und Kohlenstoff durchgesetzt, wobei der Kohlenstoff leicht verbrannt werden kann und die Reaktionsprodukte dann wieder frei vorliegen. Es sind aber auch andere unzersetzt erhitzbare Salze, wie PbCl2 oder ZnBr2, und metallisches Blei eingesetzt worden.
Eine ├╝ber mehrere Tage stabile Aerosolerzeugung wurde von G├╝nther [G├╝n93] f├╝r KCl entwickelt. Die Partikel werden durch einen Verdampfungs-Kondensations-Prozess hergestellt, der in einem R├Čhrenofen stattfindet. Dort wird das Salz auf Temperaturen von 130 oC unterhalb des Schmelzpunktes aufgeheizt. Der Vorgang der Aerosolbildung erfolgt durch Kondensatkeimbildung, Kondensation von Molek├╝len an den Keimen und durch Koagulation der gebildeten Partikel in den k├╝hleren Regionen des R├Čhrenofens. Ein entscheidender Parameter f├╝r die Transportausbeute des Gasjets ist die Gr├Č├¤enver┬Łteilung der Aerosole. Zu kleine Partikel (< 10 nm) gehen zum gro├¤en Teil durch Diffusion aus dem Gasstrom verloren [Fuc64]. Dagegen erleiden die gro├¤en Partikel Verluste durch die st├żrker wirkende Zentrifugalkraft und durch Sedimentation an Schlauch┬Łwindungen. Die Gr├Č├¤enverteilung der Aerosolpartikel kann ├╝ber die Temperatur des Ofens und den Gasfluss beeinflusst werden. Unter der Annahme einer Lognormal-Verteilung [Hin82] hat die Gr├Č├¤enverteilung unter den verwendeten Bedingungen ihr Maximum bei 100 nm und die mittlere geometrische Standardabweichung liegt bei 1,5 [G├╝n92].
Die Teilchenzahldichte und damit die Oberfl├żche, ist eine wichtige Gr├Č├¤e f├╝r die Anlagerung der R├╝cksto├¤atome [Cha91, G├╝n97]. Sie hat aber vor allem Einfluss auf die Aufladung der Partikel [Haa78, G├╝n97] in der R├╝cksto├¤kammer, die insbesondere bei hohen Projektilstrahlstr├Čmen zu Einbussen in der Transportausbeute f├╝hrt.
G├╝nther [G├╝n97] hat dazu verschiedene Gegenma├¤nahmen getestet. Dazu z├żhlte der Einsatz verschiedener (leitender oder nicht leitender) Kapillarmaterialien ebenso, wie der Zusatz verschiedener L├Čschgase zum Tr├żgergas. T├╝rler hat dazu eine Graphitspitze hinter das Target in die R├╝cksto├¤kammer eingebaut, um Ladungen abzuleiten [T├╝r00].
Alle diese Versuche waren bisher wenig erfolgreich. Deshalb scheint auch bei einer Steigerung der Projektil-Strahlstr├Čme mit neuen Beschleunigern oder mit neuen Targettechniken die Projektilstrahlstrom-Abh├żngigkeit der Jet-Ausbeute eine ŌĆ×├żrgerlicheŌĆ£ Limitierung darzustellen (Kapitel 5.2).
Die L├żnge der Kapillare von der Targetkammer zur Chemieapparatur ist entsprechend der N├żhe zum Beschleuniger bei verschiedenen Experimentaufbauten ganz unter┬Łschiedlich und kann bis zu 100 m betragen. Typische Transportausbeuten liegen bei bis zu 60% der erzeugten Aktivit├żt.
2.4 Chemische Untersuchungen und Einordnung in das Periodensystem
Bei der chemischen Untersuchung der Transactiniden stellt sich vorrangig die Frage nach der Einordnung dieser Elemente in das Periodensystem der chemischen Elemente. Das erste Transactinidenelement mit der Kernladungszahl 104 sollte demnach ein Element der 4. Nebengruppe sein, da die Actinidenreihe mit Lawrencium (Z=103) endet. M├Čglicherweise ver├żndern aber relativistische Effekte die Elektronenkonfiguration der Transactiniden derart, dass sie v├Čllig andere Eigenschaften und andere Valenzelektronen┬Łkonfigurationen als die Vertreter der entsprechenden Nebengruppenelemente aufzeigen. Dann m├╝ssten die Transactiniden ggf. in eine eigene ├£bergangsserie, wie die Lanthaniden und Actiniden eingeordnet werden.
Erste experimentelle Hinweise f├╝r eine Einordnung von Element 104 in die vierte Nebengruppe gab es in den thermochromatographischen Experimenten von Zvara [Zva69]. Dabei bildete Element 104 wie Zr und Hf leichtfl├╝chtige Chloride im Gegensatz zu den nicht fl├╝chtigen Actinidenchloriden. Dieses Ergebnis best├żtigte sich auch im ersten Experiment zur w├żssrigen Chemie von Silva [Sil70], bei dem gezeigt wurde, dass sich Element 104 im Gegensatz zu trivalenten und divalenten Actiniden von einer Kationenaustauschers├żule mit a-Hydroxyisobutters├żurel├Čsung eluieren l├żsst.
Experimente zur Komplexbildung mit Chloridionen von Hulet [Hul80] ergaben, dass Element 104 in 12 M HCl wie Hf anionische Chloridkomplexe bildet, w├żhrend von dreiwertigen Actiniden keine anionischen Chloridkomplexe bekannt sind.
Entsprechend seiner Stellung im Periodensystem ergibt sich die Elektronenkonfiguration von Element 104 als [Rn] 5f14 6d2 7s2 (zum Vergleich: Zr: [Kr] 4d2 5s2; Hf : [Xe] 4f14 5d2 6s2; Th [Rn] 6d27s2). Neueste Multikonfiguration Hartree-Fock Rechnungen [Per00] best├żtigen diese Elektronenkonfiguration. Rechnungen mit der Multi-Configurations Dirac-Fock (MCDF) Methode ergaben [Rn] 5f14 6d1 7s2 7p1 [Joh90]. Dieser p-Element Charakter (chemische ├ähnlichkeit zu Blei) konnte experimentell aber nicht best├żtigt werden [Zhu89].
Die bisherigen experimentellen Ergebnisse zu den Elementen 105-107 zeigen, dass diese Elemente der 5. bis 7. Nebengruppe sind, jedoch sind ihre Eigenschaften im Detail ├╝ber┬Łraschend. Das nicht-tantal├żhnliche Verhalten von Element 105 in w├żssriger L├Čsung und seine chemische ├ähnlichkeit zu Niob und dem Pseudohomologen Protactinium [Pau97] demonstriert beispielsweise, dass die chemischen Eigenschaften nicht in einfacher Weise extrapoliert werden k├Čnnen.
St├żrkere Auswirkungen relativistischer Effekte in der Elektronenh├╝lle auf das chemische Verhalten der Transactiniden werden sich wohl erst bei den ganz schweren Elementen 112, 114, 116 und 118 zeigen. So lassen theoretische Vorhersagen beispielsweise vermuten, dass die Element 112 und 114 Edelgase sind, welche in jedem Fall wesentlich fl├╝chtiger als Quecksilber und sehr schwer zu oxidieren sind [Pit75, Gra77].
2.5 Unterschiede zwischen tr├żgerfreier und tr├żgerhaltiger Chemie
Das Grundkonzept der Chemie mit Spurenmengen (ŌĆ×TracerŌĆ£) ist ganz verschieden von der Mikrochemie (z.B. in der Spurenanalytik) und grenzt sich von dieser dadurch ab, dass mit abnehmender Menge oder Konzentration einer Substanz neue Ph├żnomene und Materialeigenschaften beobachtet werden, die nicht oder nur unwesentlich unter normalen Bedingungen in Erscheinung treten [Ben80, Adl93].
Die Eigenschaften von Substanzen sowie ihre chemischen Reaktionen in w├żssrigen L├Čsungen und die daf├╝r geltenden Gesetze wurden im allgemeinen bei Konzentrationen von gr├Č├¤er 10-5 mol/L untersucht. St├żrker verd├╝nnte L├Čsungen sind eher ungew├Čhnlich in der chemischen Praxis. In diesen verd├╝nnten L├Čsungen kann die Adsorption gel├Čster Mikrokomponenten an festen Phasen (z.B. Gef├ż├¤w├żnden) beobachtet werden, Spuren┬Łkomponenten k├Čnnen nicht ausgef├żllt oder nicht mitgef├żllt werden, Kolloidbildung ist m├Čglich, u.v.m. [Lie89, Gui91]. Das bedeutet, dass sich die Konzentration in der L├Čsung mit der Zeit ├żndern kann. Auf der anderen Seite erreichen die physikalisch-chemischen Eigenschaften von sehr verd├╝nnten realen L├Čsungen die Eigenschaften von idealen L├Č┬Łsungen, z.B. wird die Aktivit├żt a einer gel├Čsten Komponente gleich ihrer Konzentration c, Diffusion und elektrophoretische Mobilit├żt werden unabh├żngig von der Konzentration. Folglich kann man L├Čsungen mit einer Konzentration von kleiner 10-5 M (bei einem relativen Atomgewicht von 100 entspricht das einer Konzentration von 1 mg/mL) als unendlich verd├╝nnte L├Čsungen betrachten. Adloff und Guillaumont sprechen ab einer Konzentration von 10-10 M von ŌĆ×tracer-scale chemistryŌĆ£.
Die Chemie der Spurenmengen ist eine Dom├żne der Radiochemie, da die Detektion von geringsten Mengen durch hochsensitive Strahlungsmessungen relativ einfach m├Čglich ist. So entspricht eine gut messbare Aktivit├żt von 10 Bq 241Am (T1/2=432 a) einer Menge von 3*10-11 g (gel├Čst in 1 mL entspricht das einer Konzentration von 3*10-10 M). Dabei ist der Einsatz von ├╝ber Kernreaktionen zug├żnglichen tr├żgerfreien Nukliden m├Čglich, aber auch die Verwendung von neutronenaktivierten Verbindungen erreicht diesen Konzen┬Łrationsbereich. Durch Zugabe von inaktivem Tr├żger ist die Verkn├╝pfung des Bereiches der Tracerkonzentration und der ŌĆ×normalenŌĆ£ Chemie m├Čglich.
Beide oben beschriebenen Effekte sind rein physikalisch-chemischer Natur, so dass davon ausgegangen werden kann, dass sich das Verhalten von Tracermengen in Bezug auf die ionische Komplexbildung und damit das chemische Verhalten bei einfachen Systemen nicht auswirkt. Die kinetischen Effekte bei Komplexbildungsreaktionen werden danach auch klein sein; sie sind aber ohne Zweifel vorhanden.
2.6 Thermodynamik und Kinetik in der Chemie einzelner Atome
Neben der Fragestellung nach dem unterschiedlichen chemischen Verhalten von Mikro- und Makrokomponenten stellt sich weiterhin die Frage, inwieweit das Verhalten eines einzelnen Atoms immer noch repr├żsentativ f├╝r das Verhalten eines Elements ist. Das ist auch eine Frage, ob die statistische Beschreibung der Thermodynamik in diesem Bereich noch g├╝ltig ist und die Kinetik der chemischen Reaktion schnell genug ist, damit chemische Reaktionen mit den zu untersuchenden kurzlebigen Spezies ├╝berhaupt ablaufen.
Da ein einzelnes Atom zur gleichen Zeit nie in unterschiedlichen chemischen Formen eines chemischen Gleichgewichts stehen kann, ersetzen Guillaumont und Adloff in ihrer grundlegenden Arbeit [Gui89] f├╝r einzelne Atome die klassische Zustandsfunktion durch eine Einteilchenzustandsfunktion und die Konzentration durch Wahrscheinlichkeiten, dass sich das Atom in dem einen oder anderen Zustand (Phase) befindet. Demnach l├żsst sich ein Verteilungskoeffizient auf der Basis von Wahrscheinlichkeiten definieren. Um eine statistisch signifikante Aussage zu erhalten, muss der Vorgang der Verteilung mehrfach wiederholt werden. Das hei├¤t in der Praxis, dass ein Einstufenprozess viele sich st├żndig wiederholende Einzelexperimente erfordert. Wird jedoch eine dynamische Verteilung w├żhrend eines Experiments untersucht, bei der (wie bei chromatographischen Verfahren) eine Vielzahl gleicher Einstufenprozesse (zwischen station├żrer und mobiler Phase) aufeinanderfolgen, so liegt im Ergebnis ebenfalls eine statistische Aussage ├╝ber das Verhalten eines einzelnen Atoms vor.
Soll das Fehlen einer hinreichend gro├¤en Zahl von Teilchen dadurch kompensiert werden, dass das einzelne Atom innerhalb seiner Lebensdauer viele Hin- und R├╝ckreaktionen des chemischen Gleichgewichts durchl├żuft, seine chemische Form also mit einer sehr hohen Frequenz von Hunderten oder Millionen von Austauschprozessen pro Sekunde st├żndig wechselt, ist nach Borg und Dienes [Bor81] ein chemisches System zu w├żhlen, das eine Aktivierungsenergie unterhalb von 72 kJ besitzt. Unter diesen Bedingungen ist die Aufenthaltszeit des einzelnen Atoms in beiden am chemischen Gleichgewicht beteiligten Zust├żnden so kurz, dass das Gleichgewicht innerhalb weniger Sekunden erreicht wird. Ist das Gleichgewicht erreicht, ist die fraktionale mittlere Zeit, die das Atom in einem der beiden Zust├żnde verbringt, proportional zum Wert der Gleichgewichtskonstanten. Das hei├¤t, eine experimentelle Bestimmung der relativen H├żufigkeit, mit der sich das einzelne Atom in dem einen oder anderen Zustand befindet, wird eine Gleichgewichtskonstante ergeben, die der von Makromengen entspricht.
5.1 Gasjet und Targetaufbau am Beschleuniger
Der Aufbau des Gasjetsystems wird im Prinzip an anderer Stelle auf www.kernchemie. de beschrieben (Systeme am TRIGA-Forschungsreaktor). Das Targetmaterial, z.B. Curium-248, wird nach chemischer Reinigung von Pb aus einer Cm(NO3)3-L├Čsung auf einer Beryllium-Tr├żgerfolie (Dicke etwa 15 mm) durch molecular plating in Isopropanol abgeschieden. Typische Target┬Łdicken sind zwischen 500 und 1000 mg/cm2. Das Target wird zu Beginn mit einer geringen Strahlintensit├żt bestrahlt (ŌĆ×eingebackenŌĆ£). Dabei bildet das Oxid eine glasartige Modifikation, die bei der weiteren intensiven Bestrahlung mit Schwerionen stabil bleibt. Diese Einbackprozedur verringert auch, dass sp├żter Targetmaterial in gr├Č├¤erem Umfang mit dem Schwerionenstrahl abgesputtert wird, was im laufenden Experiment ggf. durch Curium-Kontaminationen bei der a-Spektroskopie st├Čren k├Čnnte.
Das Targetmaterial wird mit dem Backing zum Strahl hin eingebaut. Bei einem statio┬Łn├żren Target wird die R├╝ckseite mit einem Stickstoffstrom gek├╝hlt (Abbildung 24). Bei diesem Mehrkammersystem wird die Druckdifferenz zwischen Beschleunigervakuum und gasgef├╝llter R├╝cksto├¤kammer stufenweise abgebaut. Die Fenstermaterialien (Beryllium oder HAVAR├ó) limitieren dabei den Staudruck in der R├╝cksto├¤kammer, der durch das str├Čmende Transportgas erzeugt wird.
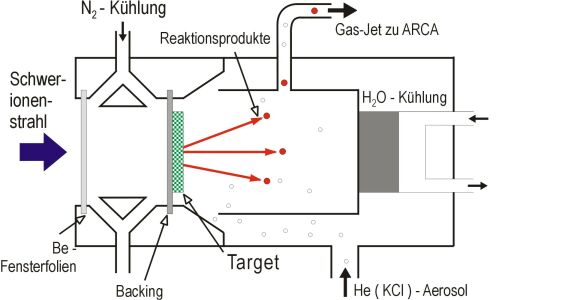
Abb.24: Targetaufbau an einem Schwerionenbeschleuniger
Die f├╝r die Experimente verwendete R├╝cksto├¤kammer hat einen Au├¤endurchmesser von 177 mm und eine L├żnge von 256 mm. Das Innenvolumen, das vom Gasjet durchsp├╝lt wird, betr├żgt aber nur 98 mL. Die mit dem Schwerionenstrahl gebildeten R├╝cksto├¤atome werden in dem Gasraum der R├╝cksto├¤kammer abgebremst und lagern sich an die Aerosole des Gasjets an. Die Projektile, die nicht mit dem Target zur Fusionsreaktion f├╝hren, werden im wassergek├╝hlten Beamdump gestoppt. An dieser Stelle wird dann auch der experimentelle Strahlstrom als elektrischer Strom detektiert.
Beim station├żren Target wird der intensive Ionenstrahl durch einen Wobbler auf die Targetfl├żche verteilt, damit es nicht zu lokalen ├£berhitzungen des Targets kommt. H├Čhere Ionenstrahlintensit├żten erm├Čglicht ein drehendes Targetrad, bei dem das Target in Bananenform am Rand einer rotierenden Scheibe befestigt wird. Der Ionenstrahl ├╝berstreicht damit eine gro├¤e Fl├żche und die im Target deponierte Energie wird ├╝ber das gesamte Targetrad verteilt. Hier kann auf die Stickstoffk├╝hlung verzichtet werden.
6.5 Kd-Wert-Bestimmung mit ARCA
ARCA (Automatic Rapid Chemistry Apparatus) wurde entwickelt, um eine gro├¤e Anzahl von HPLC-Experimenten in schneller Folge teilautomatisiert durchf├╝hren zu k├Čnnen [Sc├ż89]. Ventile und Schieber dieses Aufbaus k├Čnnen computergesteuert mit Pressluft-Zylindern einzeln angesprochen und bewegt werden, ebenso wie verschiedene HPLC-Pumpen (P1-P3) computergesteuert angesprochen werden, die mit einem konstanten Fluss unterschiedliche L├Čsungen in das System einspeisen.
![]() Beschreibung der Apparatur unter www.kernchemie.uni-mainz.de (Arbeitskreis J.V. Kratz)
Beschreibung der Apparatur unter www.kernchemie.uni-mainz.de (Arbeitskreis J.V. Kratz)
[1] Pseudohomolog deshalb, da die Einordnung der Transactiniden in die 7. Periode nicht absolut gesichert ist. Thorium ist ein Element der Actinidenserie.
[2] Zur Entdeckung von Element 118 f├╝hrte die Beobachtung von 3 Zerfallsketten, bei denen 293118 eine Lebensdauer von etwa 240 ms aufweist. Ein neues Element gilt nach der IUPAC Transfermiumelement-Working Group als entdeckt, wenn der Compoundkern 10-14 s ŌĆ×├╝berlebtŌĆ£. Diese Zeit ist notwendig, um eine Elektronenh├╝lle auszubilden.
[3] 298114 zerf├żllt in der beobachteten Zerfallskette in ein 15,4 min-Isotop des Elements 112 und weiter in ein 1,6 min-Isotop von 110 und schlie├¤lich in ein 16,5 min-Isotop von Element 108.
Der Text wurde editiert aus der Dissertation von Andreas Kronenberg. Die Zitate sind in der Originalarbeit abrufbar, die als elektronische pdf-Version von der Bibliothek der Universti├żt Mainz zur Verf├╝gung gestellt wird.


Living textbook
of Nuclear Chemisty
